近日,我校江蘇省中藥高效給藥系統工程技術研究中心王若甯教授、狄留慶教授團隊在Acta Pharmaceutica Sinica B、Journal of Controlled Release和Nano Today上發表系列成果,利用細胞外囊泡作為藥物遞送系統應用于腦膠質瘤的免疫治療。細胞外囊泡具有高生物相容性、細胞特異性、更好的穩定性和有限的免疫原性等優勢,因此被廣泛應用于腫瘤治療藥物遞送系統。此外,細胞外囊泡還能夠調節免疫抑制性腫瘤微環境,從而激活免疫反應,抑制腫瘤進展。
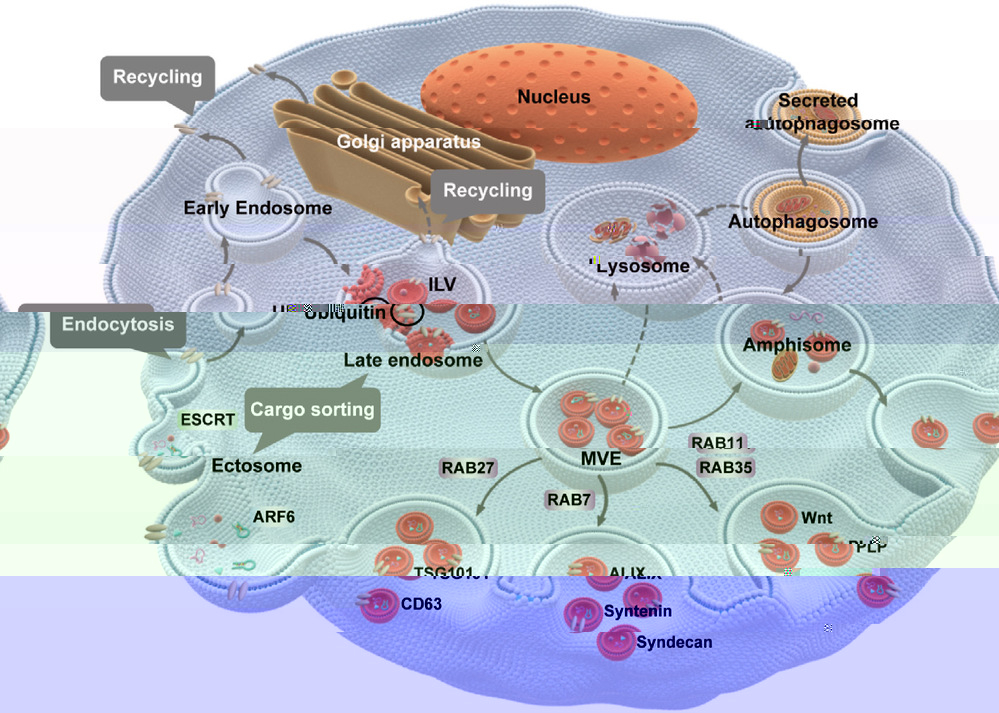
基于細胞外囊泡在細胞間通訊、促進細胞遷移和協調免疫反應中發揮重要作用,并且是藥物遞送的優良天然載體,課題組綜述了不同來源的細胞外囊泡作為生物标志物和藥物遞送系統在腫瘤治療中的重要作用及其逆轉免疫抑制微環境作用,并發表在知名期刊Acta Pharmaceutica Sinica B(中科院一區,IF:14.6),題為Extracellular vesicles as biomarkers and drug delivery systems for tumor。
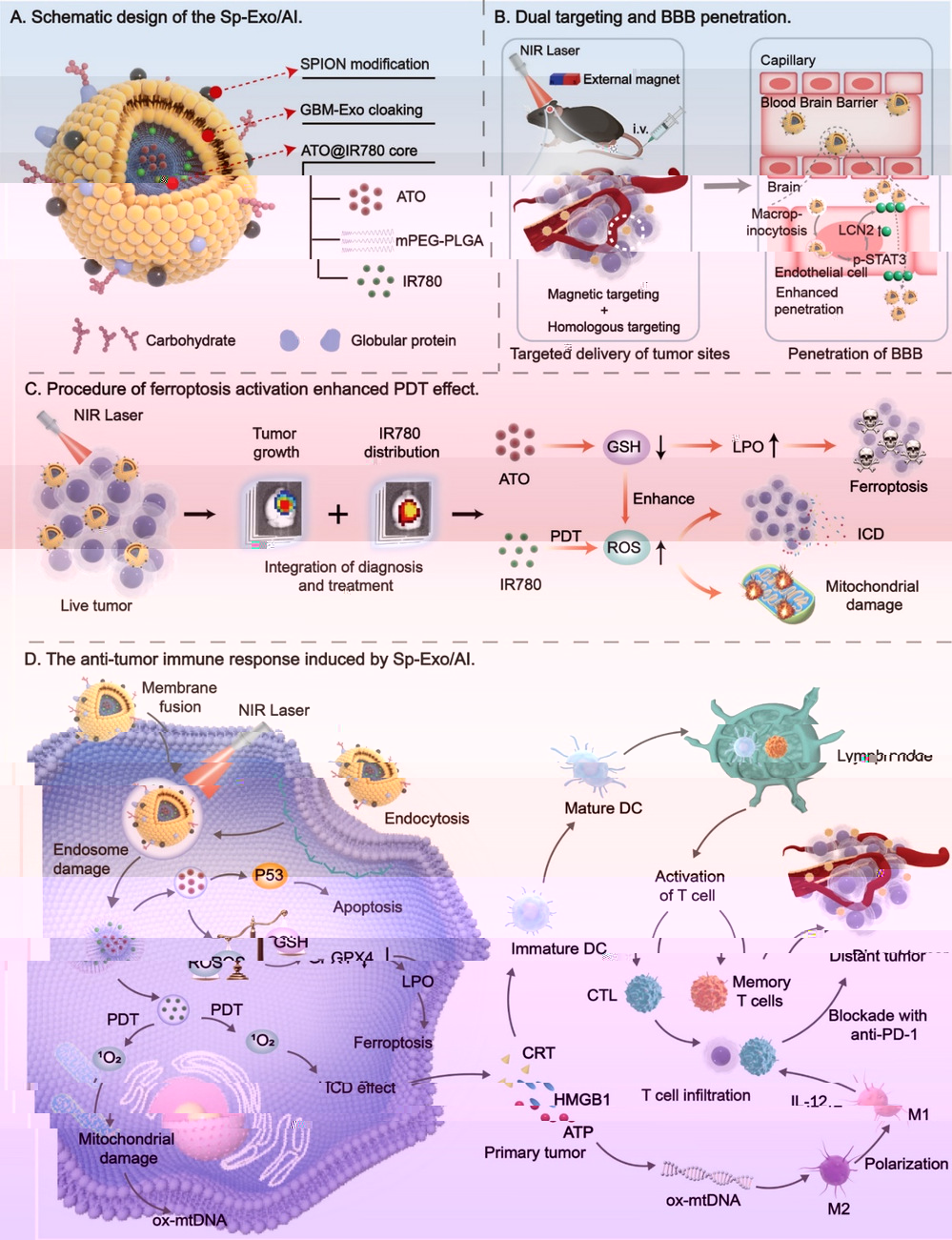
2025年5月2日,團隊在知名期刊Journal of Controlled Release(中科院一區,IF:11.5)上發表題為“Homologous magnetic targeted immune vesicles for amplifying immunotherapy via ferroptosis activation augmented photodynamic therapy against glioblastoma”的研究性論文,針對細胞外囊泡的天然腫瘤靶向能力為腦膠質瘤的治療提供新策略。
腦腫瘤藥物的遞送及治療面臨血腦屏障滲透率低及免疫“冷”特征,因此,研究團隊基于腫瘤來源外泌體開發了一種同源磁性靶向免疫囊泡,負載的中藥砒霜活性成分三氧化二砷通過鐵死亡激活,增強光動力療法促進先天性和适應性免疫。Sp-Exo/AI通過同源歸巢和磁導航的大腦雙重靶向促進BBB跨越和藥物腫瘤積累。經激光照射後,Sp-Exo/AI産生大量ROS,誘導T細胞活化及腫瘤相關巨噬細胞的極化,并聯合αPD-1激活效應記憶T細胞從而克服腫瘤免疫逃逸,顯著抑制腦膠質瘤生長及複發。
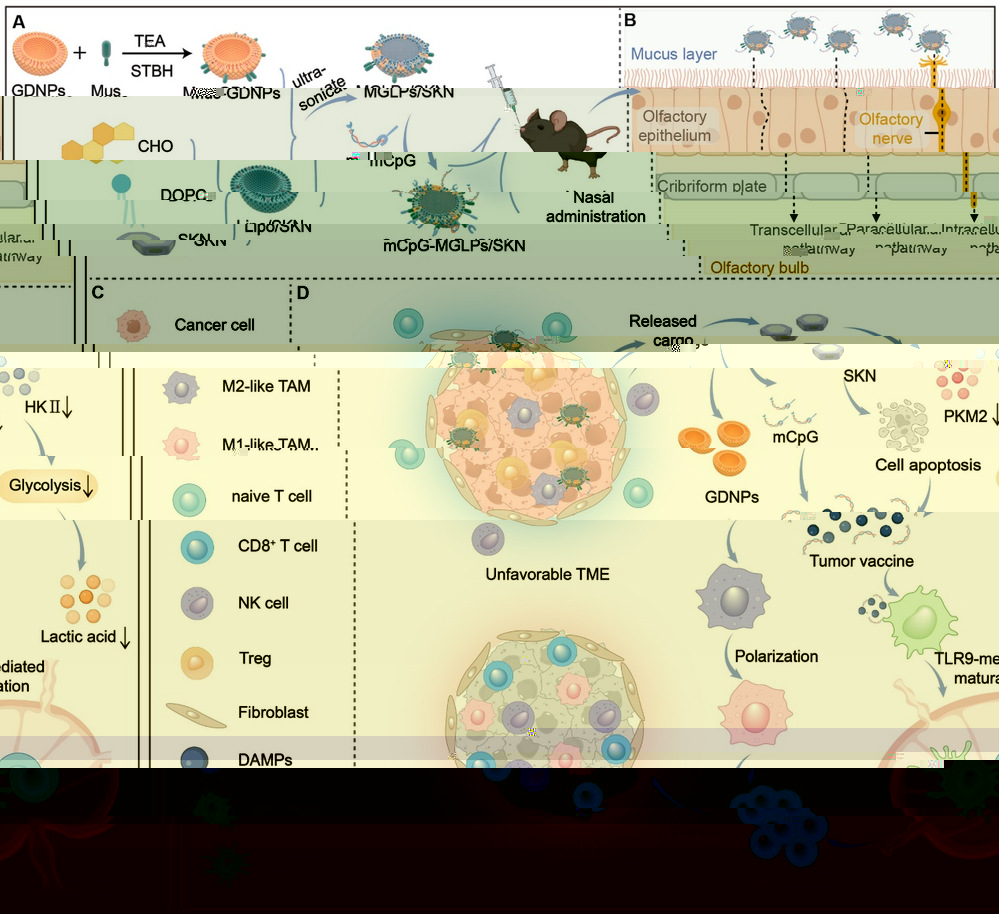
6月15日,團隊在知名期刊Nano Today(中科院一區,IF:13.2)上發表題為“Intranasal hybrid vesicles delivering personalized in situ nano-vaccines induce glioblastoma remodeling to sensitize immunotherapy”的研究性論文,通過中草藥來源細胞外囊泡調節腫瘤微環境,為腦膠質瘤的免疫治療提供新方向。
腦膠質瘤的免疫抑制還由糖酵解的過度激活驅動,其代謝産物乳酸的積累促進腫瘤相關巨噬細胞向免疫抑制M2表型轉化。因此,課題組提出了一種基于人參囊泡的雜交囊泡原位納米疫苗,其可通過經鼻遞送繞過血腦屏障,增強腫瘤免疫應答的同時抑制糖酵解代謝。人參皂苷Rg3發揮靶向腦腫瘤的作用,随後中藥紫草活性成分紫草素誘導免疫原性細胞死亡同時抑制糖酵解限速酶PKM2和HK II,協同人參囊泡的腫瘤相關巨噬細胞極化作用,為先天和适應性免疫誘導提供了一種多管齊下的方法。
上述研究得到了國家重大人才工程青年項目,國家自然科學基金(No. 82274104, 82074024, 82374042),江蘇省優秀青年基金(No. BK20240144),中藥制藥過程控制與智能制造技術全國重點實驗室科研創新項目(No. NZYSKL240103),bevictor伟德官网标志性人才培育項目(No. RC202407) 等項目的資助。
原文鍊接:
https://doi.org/10.1016/j.apsb.2025.04.033
https://doi. org/10.1016/j.jconrel.2025.113816
https://doi:10.1016/j.nantod.2025.102840



